Gaz - puzzle online










































Puzzle online Gaz
Gaz
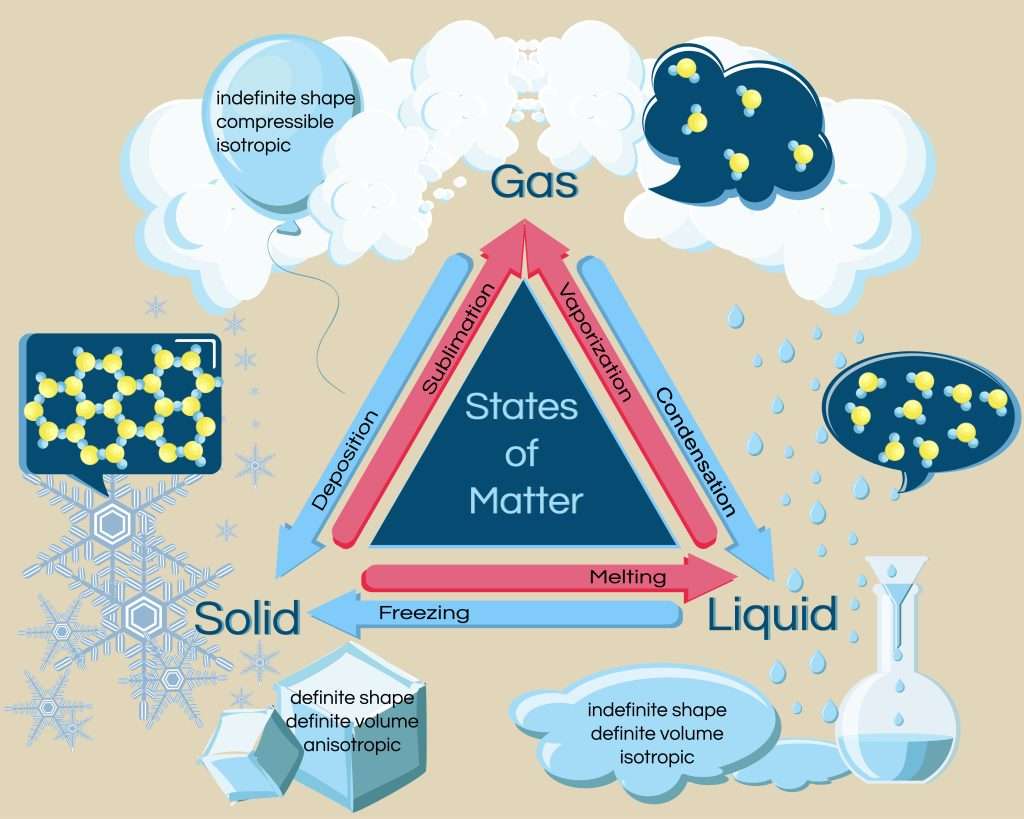
Gaz – stan skupienia materii, w którym ciało fizyczne łatwo zmienia kształt i zajmuje całą dostępną mu przestrzeń. Właściwości te wynikają z własności cząsteczek, które w fazie gazowej mają pełną swobodę ruchu. Wszystkie one cały czas przemieszczają się w przestrzeni zajmowanej przez gaz i nigdy nie zatrzymują się w jednym miejscu. Między cząsteczkami nie występują żadne oddziaływania dalekozasięgowe, a jeśli, to bardzo słabe. Jedyny sposób, w jaki cząsteczki na siebie oddziałują, to zderzenia. Oprócz tego, jeśli gaz jest zamknięty w naczyniu, to jego cząsteczki stale zderzają się ze ściankami tego naczynia, wywierając na nie określone i stałe ciśnienie.
Termin wprowadzony przez flamandzkiego lekarza Johanna Helmonta w XVII wieku wzorem gr. χάος ‘cháos’.
Cząsteczki gazu przemieszczają się z różną szybkością, a rozkład tych szybkości ma charakter całkowicie statystyczny (rozkład Maxwella). Średnia szybkość poruszania się cząsteczek w gazie jest zależna wyłącznie od ich masy cząsteczkowej i temperatury. Podczas obniżania temperatury gazu maleje średnia szybkość cząsteczek, zaś zwiększanie ciśnienia powoduje zmniejszenie średniej odległości między nimi. Obniżanie temperatury lub zwiększanie ciśnienia prowadzi w końcu do skroplenia lub resublimacji gazu. Zamiana gazu w ciecz lub ciało stałe wynika z faktu, że w pewnym momencie energia oddziaływań międzycząsteczkowych (sił van der Waalsa, wiązań wodorowych itp.) staje się większa od energii kinetycznej cieplnego ruchu cząsteczek.
W fizyce przyjmuje się często prosty model gazu doskonałego, w którym cząsteczki gazu nie przyciągają się i nie mają objętości własnej. Teorie i zależności termodynamiczne wywiedzione z założeń gazu doskonałego sprawdzają się dość dobrze (na ogół) w przypadku niezbyt dużych ciśnień oraz niezbyt niskich temperatur. W innych przypadkach prawa te jednak zawodzą i wtedy stosuje się bardziej złożone modele gazów i tworzy dokładniejsze teorie i zależności (zob. gaz rzeczywisty, równanie van der Waalsa, wirialne równanie stanu).
Interesującą cechą gazu (a ściślej gazu doskonałego) jest to, że objętość przez niego zajmowana (w danej temperaturze i ciśnieniu) jest stała, niezależnie od rodzaju cząsteczek, jakie są w gazie, i zależy wyłącznie od liczby tych cząsteczek. Innymi słowy, jeśli weźmiemy np. 1 litr wodoru i 1 litr tlenu (oba przy tym samym ciśnieniu i temperaturze), to w obu objętościach będzie dokładnie taka sama liczba cząsteczek. Jest to tzw. prawo Avogadra.
Aby jednoznacznie określić stan gazu, poza składem chemicznym (ułamki wagowe lub molowe) i temperaturą należy podać gęstość gazu lub jego ciśnienie. Zamiast gęstości można podać równoważnie objętość molową lub stężenie gazu.
Dla dowolnego gazu:
objętość jednego mola gazu w warunkach normalnych: V = 22,4 dm³
liczność gazu w (liczba moli):
n
=
N
N
a
=
m
M
n={\frac {N}{N_{a}}}={\frac {m}{M}}
stężenie molowe gazu:
C
m
=
n
V
C_{m}={\frac {n}{V}}
objętość molowa gazu:
V
m
=
V
n
V_{m}={\frac {V}{n}}
gdzie: m – masa gazu, V – objętość gazu, N – liczba cząsteczek, NA – liczba Avogadra, M – masa molowa.
Dla gazu doskonałego:
p
=
C
m
R
T
p=C_{m}RT
p
=
ρ
(
R
T
M
)
p=\rho {\begin{pmatrix}{\frac {RT}{M}}\end{pmatrix}}
gdzie: R – uniwersalna stała gazowa, T – temperatura.
